亚硝酸钠滴定法(亚硝酸钠滴定法的注意事项)-ag8亚洲国际集团
1.亚硝酸钠滴定法的注意事项
1.将滴定管尖端插入液面2/3处进行滴定,是一种快速滴定法。
2.重氮化温度应在15~30℃,以防重氮盐分解和亚硝酸逸出。
3.重氮化反应须以盐酸为介质,因在盐酸中反应速度快,且芳伯胺的盐酸盐溶解度大。在酸度为1~2mol/l下滴定为宜。
4.近终点时,芳伯胺浓度较稀,反应速度减慢,应缓缓滴定,并不断搅拌。
5.永停仪铂电极易钝化,应常用浓硝酸(加1~2滴三氯化铁试液)温热活化。
6.亚硝酸钠滴定液应于玻塞棕色玻璃瓶中避光保存。
2.采用亚硝酸钠滴定法测定药物含量时 应注意哪些主要条件
用氧化还原滴定法测定药物含量应注意: ⑴加入掩蔽剂。
当注射剂中加入了亚硫酸钠或亚硫酸氢钠作抗氧剂时,如采用碘量法、铈量法或亚硝酸钠滴定法测定注射剂中的主药时, 这些抗氧剂会产生干扰作用, 使测定结果偏高。加入掩蔽剂丙酮或甲醛,可消除干扰。
⑵加酸分解。亚硫酸钠、亚硫酸氢钠及焦亚硫酸钠均可被强酸分解,产生二氧化碳气 体,经加热可全部逸出,除去。
⑶加入弱氧化剂氧化。可以加入一种弱氧化剂将亚硫酸盐或亚硫酸氢钠氧化,排除干 扰作用。
常用的氧化剂有过氧化氢和硝酸。 ⑷利用主药和抗氧剂紫外吸收光谱的差异进行测定。
3.亚硝酸钠的滴定条件有哪些?
亚硝酸钠在盐酸存在条件下与具有芳伯氨基化合物发生重氮化反应,定量生成重氮盐。
滴定条件: (1) 过量盐酸:加快反应速度,重氮盐在酸性条件下稳定,防止偶氮化合物形成;酸度过高会阻碍芳伯氨基游离 (2) 室温(℃~30℃)条件:温度过高使亚硝酸逸失,过低反应速度太慢 (3) 滴定时加入kbr作为催化剂 考试大-中国教育考试门户网站() (4) 滴定方式:开始时滴定管尖端插入液面下,在搅拌下迅速加入,避免亚硝酸损失。
近终点时滴定管提出液面,淋洗、缓慢滴定。 (5) 终点指示法:永停滴定法 亚硝酸钠滴定液使用基准对氨基苯磺酸标定。
4.常用的亚硝酸钠滴定法测定条件的要求
以亚硝酸钠液为滴定液的容量分析法称为重氮化法(亦亚硝酸钠法)。
原理:
芳香伯胺类药物,在盐酸存在下,能定量地与亚硝酸钠产生重氮化反应。依此,用已知浓度的亚硝酸钠滴定液滴定(用永停法指示终点),根据消耗的亚硝酸钠滴定液的浓度和毫升数,可计算出芳伯胺类药物的含量。
反应式: arnh2 nano2 2hcl→[ar-n ≡n]cl- nacl 2h2o
滴定条件:
1.酸的种类及浓度
(1)重氮化反应的速度与酸的种类有关,在hbr中比在hcl中为快,在hno3或h2so4中则较慢,但因hbr的价格较昂,故仍以hcl最为常用。此外,芳香伯胺类盐酸盐的溶解度也较大。
(2)重氮化反应的速度与酸的浓度有关,一般常在1~2mol/l酸度下滴定,这是因为酸度高时反应速度快,容易进行完全,且可增加重氮盐的稳定性。如果酸度不足,则已生成的重氮盐能与尚未反应的芳伯胺偶合,生成重氮氨基化合物,使测定结果偏低。
[ar-n ≡n]cl- arnh2→ar-n=n-nh-ar hcl
当然,酸的浓度也不可过高,否则将阻碍芳伯胺的游离,反而影响重氮化反应的速度。
2.反应温度
重氮化反应的速度随温度的升高而加快,但生成的重氮盐也能随温度的升高而加速分解。
[ar-n ≡n]cl- h2o→ar-oh n2↑ hcl
另外,温度高时hno2易分解逸失,导致测定结果偏高。实践证明,温度在15℃以下,虽然反应速度稍慢,但测定结果却较准确。如果采用“快速滴定”法,则在30℃以下均能得到满意结果。
3.滴定速度:
快速滴定法:
将滴定管的尖端插入液面下约2/3处,用亚硝酸钠滴定液迅速滴定,随滴随搅拌,至近终点时,将滴定管的尖端提出液面,用少量水淋洗尖端,洗液并入溶液中,继续缓缓滴定,至永停仪的电流计指针突然偏转,并持续1分钟不再回复,即为滴定终点。
4.苯环上取代基团的影响
苯胺环上,特别是在对位上,有其它取代基团存在时,能影响重氮化反应的速度。
(1)亲电子基团,如-no2、-so3h、-cooh、x等,使反应加速。
(2)斥电子基团,如-ch3、-oh、-or等,使反应减慢。
(3)对于慢的重氮化反应常加入适量kbr加以催化。
5.亚硝酸钠滴定法的原理,测定的主要条件及指示终点的方法有哪些
一、基本原理
亚硝酸钠在盐酸存在条件下与具有芳伯氨基化合物发生重氮化反应,定量生成重氮盐。根据亚硝酸钠的消耗量可计算出药物有效成分的含量。
二、条件
1、酸的种类及浓度
(1)重氮化反应的速度与酸的种类有关,在hbr中比在hcl中为快,在硝酸或硫酸中则较慢,但因hbr的价格较昂,故仍以hcl最为常用。此外,芳香伯胺类盐酸盐的溶解度也较大。
(2)重氮化反应的速度与酸的浓度有关,一般常在1~2mol/l酸度下滴定,这是因为酸度高时反应速度快,容易进行完全,且可增加重氮盐的稳定性。
如果酸度不足,则已生成的重氮盐能与尚未反应的芳伯胺偶合,生成重氮氨基化合物,使测定结果偏低。当然,酸的浓度也不可过高,否则将阻碍芳伯胺的游离,反而影响重氮化反应的速度。
2、反应温度
重氮化反应的速度随温度的升高而加快,但生成的重氮盐也能随温度的升高而加速分解。
三、指示终点的方法
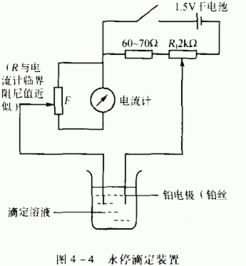
(1)永停滴定法: chp、bp多采用
主要原理:nano₂滴定时,达终点前,nano₂产生的hno₂用于重氮化反应,不与电极作用,检流计无电流通过不偏转;达到终点时,溶液中微量hno₂即会使电极起氧化还原反应,检流计指针突然偏转,且不再回复。优点:简单,方法准确缺点:电极易钝化。
(2)电位法:usp多用
原理:采用电位计,甘汞-铂电极系统。当到达终点时,溶液中多余的hno2使电位产生突跃,如用直流式电位计,则可使电位计指针突然偏转而指示终点。
(3)外指示剂法:
原理:常采用ki-淀粉糊剂或试纸(液)指示终点。滴定终点时,稍过量的nano₂在酸性液中氧化ki,析出i₂遇淀粉显兰色。
扩展资料
注意事项:
1、将滴定管尖端插入液面2/3处进行滴定,是一种快速滴定法。
2、重氮化温度应在15~30℃,以防重氮盐分解和亚硝酸逸出。
3、重氮化反应须以盐酸为介质,因在盐酸中反应速度快,且芳伯胺的盐酸盐溶解度大。在酸度为1~2mol/l下滴定为宜。
4、近终点时,芳伯胺浓度较稀,反应速度减慢,应缓缓滴定,并不断搅拌。
5、永停仪铂电极易钝化,应常用浓硝酸(加1~2滴三氯化铁试液)温热活化。
6、亚硝酸钠滴定液应于玻塞棕色玻璃瓶中避光保存。
参考资料来源:搜狗百科-亚硝酸钠滴定法
参考资料来源:搜狗百科-亚硝酸钠法
声明:本网站尊重并保护知识产权,根据《信息网络传播权保护条例》,如果我们转载的作品侵犯了您的权利,请在一个月内通知我们,我们会及时删除。
ag8亚洲国际集团 copyright © 2016 ag8亚洲国际集团. 页面生成时间:3.974秒